Перевод статьи "Psychiatric face of COVID-19" Автора Luca Steardo Jr., Luca Steardo & Alexei Verkhratsky
В рамках программы распространения информации, связанной с борьбой с коронавирусной болезнью COVID-19 и ее последствиями:
UNIVERSUM.CLINIC публикует переводы на русский язык наиболее основательных, актуальных и интересных (на наш взгляд) медицинских материалов.
Для информационной вовлеченности медицинского сообщества Украины в современные мировые тенденции и повышения уровня медицинского образования общества в целом.
Ссылка на оригинал: https://www.nature.com/articles/s41398-020-00949-5.pdf
Перевод на русский: Наталия Зохнюк / UNIVERSUM.CLINIC
Содержание
Аннотация
Введение: инфекционные пандемии как фактор риска для психических заболеваний
Нейротропизм коронавирусов
Нейрозожжение при COVID-19
COVID-19 и большое депрессивное расстройство
COVID-19 и биполярное расстройство (БР)
COVID-19 и реактивный психоз
COVID-19 и обсессивно-компульсивное расстройство
COVID-19 и эпилепсия
COVID-19 и посттравматическое стрессовое расстройство
Шизофрения и вирусная инфекция
Выводы
Notes
References
Аннотация
Коронавирусная болезнь 2019 (COVID-19) представляет собой тяжелую полиорганную патологию, которая кроме сердечно-респираторных проявлений влияет на функцию центральной нервной системы (ЦНС). Тяжелый острый респираторный синдром коронавируса 2 (SARS-CoV-2), как и другие коронавирусы, демонстрирует нейротропизм; вирусная инфекция ствола мозга может осложнить течение заболевания из-за повреждения центрального сердечно-дыхательной системы. Системное воспаление, а также нейровоспалительные изменения связаны с массовым увеличением провоспалительных молекул мозга, нейроглиальной реактивностью, измененным нейрохимическим ландшафтом и патологической перестройкой нейрональных сетей. Эти органические изменения, возникающие совместно со стрессом окружающей среды, вызванным переживаниями пребывания в палатах интенсивной терапии, страхом пандемии и социальными ограничениями, способствуют развитию нервно-психических патологий, включая большое депрессивное расстройство, биполярное расстройство (БР), различные психозы, обсессивно-ком расстройство и посттравматическое стрессовое расстройство. Нейропсихиатрические последствия COVID-19 представляют серьезную клиническую проблему, которую следует учитывать при будущих сложных терапиях.
Введение: инфекционные пандемии как фактор риска для психических заболеваний
Человеческая цивилизация всегда сосуществовала с паразитарными формами, представленными бактериями и вирусами, неизменно уносившими жизнь. Когда социальные, биологические и экономические факторы совпадали, инфекции получили широкое распространение, достигнув уровня пандемии, что повлекло за собой массовые смерти и несчастья. Пандемии поколебали основы общества и изменили ход истории и мышления человечества. Тифозная лихорадка опустошила Афины в 490 г. до н.э., тем самым дав преимущество военному обществу Спарты в Пелопоннесской войне, чума Юстиниана обрекла реинкарнацию Римской империи, тогда как Черная смерть, вызванная Yersinia pestis, убившая треть населения Европы, побудила к тектоническим изменениям в экономических отношениях, которые в конечном итоге лишились крепостного права и феодализма и заложили основы Возрождения.
Последняя глобальная эпидемия испанского гриппа, повлекшая 20–50 миллионов смертей, совпала с Первой мировой войной, междоусобными конфликтами и рождением большевизма, что вместе привело к большому смятению в человечестве. Движения больших масс солдат из США принесли вирус гриппа A H1N1 в Европу, нарушение работы медицинских служб, плохая гигиена, разрушение войны и недоедание - все это повлекло за собой суперинфекцию чрезвычайно высокой смертностью.
Все основные пандемии, связанные с сильным стрессом окружающей среды, влияют на образ мышления и психологическое здоровье. Систематические исследования, направленные на выявление патогенетических механизмов, ответственных за возникновение психических заболеваний после вирусных эпидемий, начаты в 19 веке. Выдающийся английский врач Генри Холланд в 1839 г. провозгласил, что грипп отвечает за «Из выявленных нарушений психических функций почти в одинаковом соотношении тела……. Спустя восемьдесят лет Карл Мэннигер подтвердил связь между вирусными инфекциями и психической заболеваемостью: «Сто случаев психических заболеваний, связанных с гриппом в последней пандемии, были изучены в Бостонской психопатической больнице. на четыре группы: бред, деменция, другие психозы и неклассифицированные, среди них численность наибольшей группы – деменция praecox».
С годами накопленные клинические данные укрепили наши знания о психиатрических особенностях церебральных заболеваний. За последние несколько десятилетий интерес к предполагаемой этиологической роли вирусов постепенно усиливался, охватывая не только органические психические расстройства, вызванные острым вирусным энцефалитом и медленными вирусными инфекциями центральной нервной системы (ЦНС), но также охватывал так называемыми функциональными психиатрическими заболеваниями. биполярное расстройство (БР). Общепризнано, что сочетания системной инфекции, вирусного нейротропизма и стресса с окружающей среды облегчают или даже стимулируют развитие психических патологий, усугубляющих течение пандемии и представляющих значительную терапевтическую проблему.
Нейротропизм коронавирусов
Пандемия болезни коронавируса 2019 (COVID-19) возрождает давно забытый вызов для человечества, жившего в (иллюзионной) среде массового заражения. Борьба с неопределенностью недавно возникшей болезни, против которой не существует ни вакцины, ни эффективного протокола лечения, человечество скорее всего будет существовать в новой реальности месяцами, если не годами до внедрения глобального средства защиты. Каким образом вирус взаимодействует с нашим организмом и каковы патофизиологические сценарии развития острой фазы болезни и долговременные последствия - это важнейшие вопросы для решения медицинских стратегий.
COVID-19 является результатом заражения новым коронавирусом, который впервые был обнаружен в Китае после первоначальной вспышки в 2019 году. Этот коронавирус, названный тяжелым острым респираторным синдромом коронавируса 2 (SARSCoV-2), относится к группе 2B семейства β-коронавируса. SARS-CoV-2 признан седьмым компонентом семейства коронавирусов и был включен в подсемейство ортокоронавирина. Коронавирусы – это одноцепочечные РНК-вирусы, как правило, связанные с респираторными заболеваниями; они также (хотя и реже) могут вызвать желудочно-кишечные и неврологические расстройства у широкого круга млекопитающих и птиц. Коронавирусы обладают высокими показателями мутации и рекомбинации, а также склонностью к перекрестной передаче. SARS-CoV-2 попадает в клетку после связывания с ферментом АСЕ2 с последующей эндоцитарной интернализацией. Основными мишенями вируса являются эпителиальные клетки легких и желудочно-кишечного тракта.
Эндоцитоз вирусного комплекса ACE2 также приводит к истощению пула ACE2 с последующим уменьшением инверсии ангиотензина II к ангиотензину; последний пептид обладает выраженными противовоспалительными свойствами, а снижение Arg 1-7 существенно способствует легочной недостаточности и массовому возникновению легочного фиброза, описанного у пациентов с COVID-19. Может ли SARS-CoV-2 проникать в клетки через альтернативные пути, остаются непонятными, хотя в отличие от других коронавирусов, SARS-CoV-2 не связывается с рецепторами, такими как аминопептидаза N и дипептидилпептидаза.
В клинической презентации COVID-19 преобладают респираторные признаки с более редким появлением желудочно-кишечных симптомов. Инвазия вируса не ограничивается двумя органами, особенно учитывая, что значительная экспрессия АПФ2 проявляется в других тканях, включая сердце, почки, эндотелий и ЦНС. Вирусная инфекция мозга может иметь многочисленные неврологические и психиатрические последствия, способствуя как острой фазе заболевания, так и его потенциальным последствиям. Нейротропизм хорошо задокументирован для нескольких β-коронавирусов, включая SARS-CoV-1, MERS-CoV и вирус HEV 67 N свиного гемагглютинационного энцефаломиелита. Возможно, основной путь SARSCoV-2 связан с АСЕ2, экспрессированным в нейронах и нейроглии. Нейронные клетки, экспрессирующие АСЕ2, находятся вокруг вентрикулярных органов, таких как субфоникалький орган, паравентрикулярное ядро, одиночный тракт и ростральный вентролатеральный продолговатый мозг. Все эти регионы мало защищены гематоэнцефалическим барьером (ГЭБ) и все они участвуют в сердечно-сосудистой и дыхательной регуляции. Отсутствие ГЭБ делает эти участки ЦНС уязвимыми при многих патологиях, таких как различные типы системного воспаления, включая энцефалопатию, связанную с сепсисом, нейроинфекцию бактериями, вирусами или паразитами, стресс и аутоиммунный энцефалит. Микроглиальные клетки, локализованные в околовентрикулярных органах, кажется, находятся в состоянии хронической активации, пытаясь ограничить поступление в паренхиму циркулирующих нейротоксических молекул или инвазивных агентов и сохранить мозговой гомеостаз. SARS-CoV-2, подобно другим респираторным вирусам, может получить доступ к ЦНС несколькими путями, например, мигрируя через аксоны обонятельного нерва. Было показано, что интраназальная инфекция SARS-CoV-1 или MERS-CoV27 приводит к быстрому распространению вирусных частиц в мозг, возможно, из-за обонятельной луковицы путем ретроградного аксонального транспорта. Размножающиеся в носовой полости вирусы могут использовать прямую связь с обонятельной луковицей для колонизации ЦНС. В этой парадигме вирус транспортируется через аксоны нейронов обонятельной луковицы с последующим заражением специфического типа нейроглии, воспринимаемых клетками обонятельной луковицы. Когда вирус вводили интраназально в очень низких дозах, распространение было только в ЦНС, усиливая концепцию внутреннего нейротропизма коронавирусов. У грызунов абляция обонятельной луковицы предотвратила распространение вирусов после назальной инфекции.
Дальнейшая поддержка роли назально-обонятельного пути происходит от клинических наблюдений, согласно которым аносмия развивается рано у больных SARS-CoV-2. РНК SARS-CoV-2 присутствовала в течение 20 и более дней в образцах секреции ротоглотки и носоглотки 30% людей, переживших COVID-19, предполагая, что SARS-CoV-2 может длительное время задерживаться как на верхних, так и нижних дыхательных. путях.
Вирус также может попасть в мозг из-за заражения эндотелиальных клеток, выстилающих сосудистую систему мозга. Электронно-микроскопический анализ лобной частицы выявил вирусные частицы SARS COV-2 в эндотелии с некоторыми показаниями относительно транзита вируса к нейропилю. SARSCov-2 может попадать в ЦНС посредством периваскулярных пространств лимфатической системы. Кроме того, вирусы могут вторгаться в мозг через другие нервы, такие как тройничный нерв, проектирующий ноцицептивные окончания в носовые полости. Подобным образом сенсорные волокна блуждающего нерва, иннервирующие дыхательные пути, могут представлять другой путь инвазии.
Последующие доказательства нейроинфекции SARS-CoV-2, отеков и нейрональной дегенерации были зарегистрированы в образцах мозга после смерти, тогда как в случае секвенирования генома энцефалита подтверждено наличие вируса в ликворе. Послесмертный анализ нервной ткани из ткани 54-летнего мужчины, умершего от тяжелой дыхательной недостаточности, ассоциированной с COVID-19, выявил вирусные частицы SARS-COV-2 в обонятельном нерве, в прямой извилине и в стволе мозга с признаками глубокого повреждения всех элементов ткани. , включая глиальные клетки, нейроны, их аксоны и миелин
Следовательно, кажется, что SARS-CoV-2, подобно SARS-CoV-1 и MERS-CoV, инфицирует ствол мозга, в котором расположены дыхательные нейронные цепи, и, по аналогии, подобная инфекция может происходить и способствовать дыхательной недостаточности, наблюдаемой при пневмонии SARS-CoV-2 дыхание зависит от центрального регулятора, расположенного в дорсолатеральном мосту, в ядре одиночного тракта и в вентролатеральном мозге. Этот генератор отвечает за дыхательные ритмы и контроль двигательных нейронов, иннервирующих дыхательные мышцы. В субпопуляции COVID-19 дыхательная недостаточность пациентов проявляется снижением частоты дыхания с гипоксией и гиперкапнией. Многие из этих пациентов остаются в коме в течение дней, несмотря на приостановку седативного лечения и отсутствие явных метаболических изменений, что свидетельствует о вирусном энцефалите, который часто решается без серьезных последствий. Однако это бывает не всегда, и когда степень дыхательной недостаточности чрезвычайна, пациенты умирают до того, как может оказаться очевидным повреждение мозга, вызванное вирусом.
Учитывая вирусную нагрузку на мозговой ствол, дальнейшее уменьшение экспрессии АСЕ2, связанное со смертью нейронов, может привести к изменению функции барорецепторов, связанного с повышением симпатического тонуса и серьезным, угрожающим жизни, повышением АД. Энцефалит, о котором сообщают как об осложнениях коронавирусной инфекции, неизменно поражает не только ствол головного мозга, но также таламус и белое вещество. Эти аспекты должны учитываться клиницистами, имеющими дело с пациентами с COVID-19, имеющими серьезную сердечно-сосудистую и дыхательную недостаточность. Признание того, что респираторные симптомы могут, по крайней мере, частично происходить от энцефалитического повреждения ствола мозга, может помочь разработать более эффективные методы лечения.
Повреждения ствола мозга, а также других структур мозга также могут быть результатом системного воспаления, которое часто называют синдромом системной воспалительной реакции или "бурей цитокинов". Одновременно мозг является мишенью для инфекционно-токсической энцефалопатии, ассоциированной с системной токсемией или гипоксией, сопровождающих острые инфекционные заболевания. Токсичные энцефалопатии имеют массивные неврологические и психиатрические проявления и даже отек мозга, однако развивается без накопления маркеров воспаления в спинномозговой жидкости. Кроме того, системная инфекция и высокий уровень циркулирующих цитокинов часто повреждают микроциркуляцию, вызывая отеки и тромбоз; Тромбоэмболия сообщается примерно у 30% пациентов. Кроме того, цитокины активируют вегетативные нервы и ось гипоталамус-гипофиз-надпочечники, которые влияют на артериальное давление. Все эти факторы в совокупности обуславливают ишемическое поражение мозга и связаны с возникновением инсультов, еще больше увеличивающих смертность у пациентов с COVID-19.
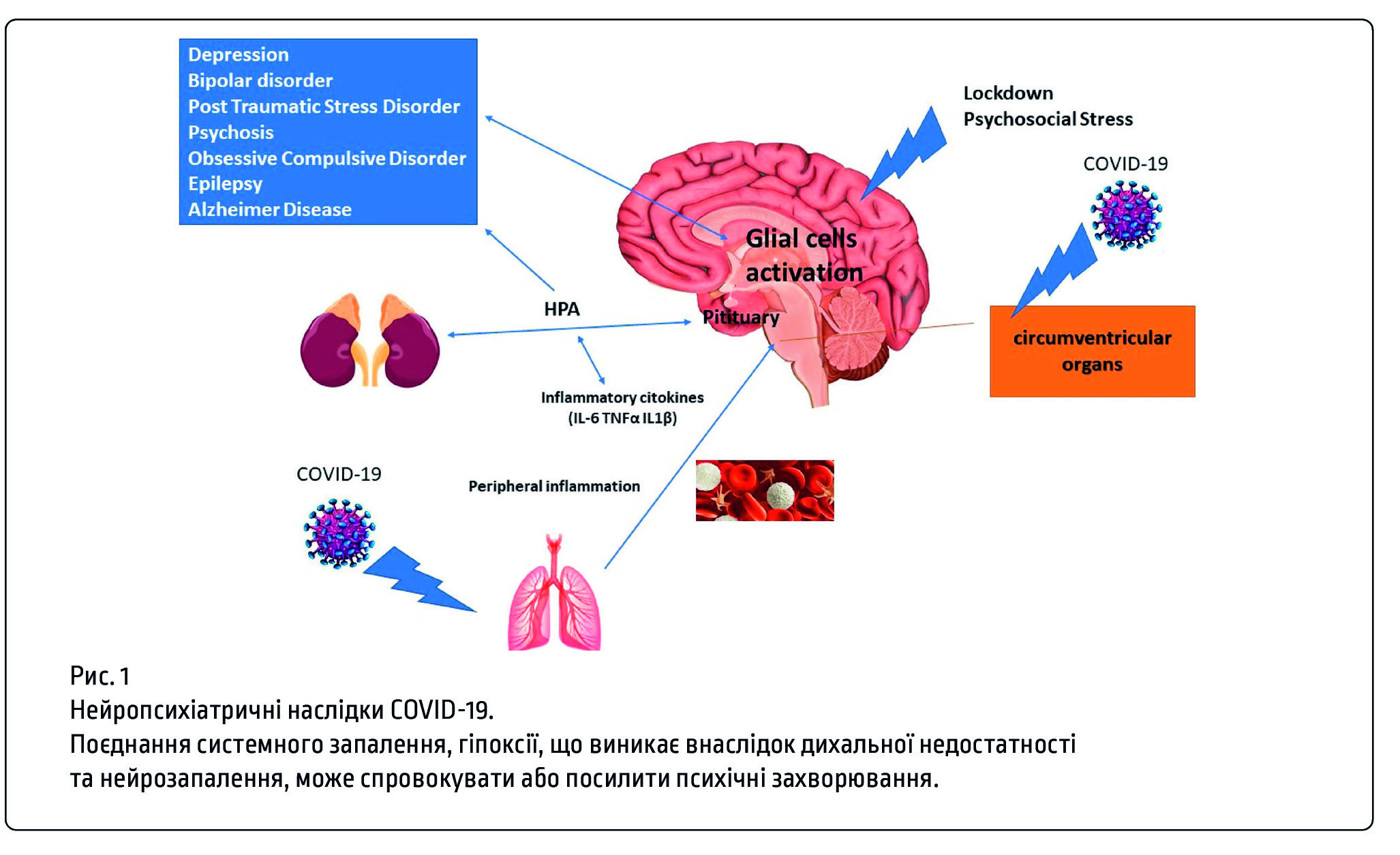
Нейровоспалене при COVID-19
Несмотря на существование ГЭБ, мозг и спинной мозг взаимодействуют с периферической иммунной системой, следовательно, каждое системное воспаление влияет на ЦНС. В контексте COVID-19 повреждение ГЭБ, опосредованное массовым увеличением циркулирующих провоспалительных факторов, очень вероятным. Нарушенный ГЭБ позволяет воспалительному шторму охватить ЦНС, что приводит к функциональным повреждениям. Попадая в мозг, периферические воспалительные молекулы, а также воспалительные клетки провоцируют нейровоспаление, тем самым нарушая гомеостаз, изменяя нейронные сети и индуцируя гибель нейронов.
На начальных фазах системного воспаления противовирусный иммунитет может эффективно притупить вирусное распространение, поскольку реактивность нейроглии и приток исследуемых Т-клеток могут удалить инфекционные элементы, предотвращая распространение без дальнейшего повреждения тканей. При тяжелом течении COVID-19 значительное высвобождение хемокинов и интерлейкинов, связанное с системным воспалением и выраженной лимфопенией, обеспечивает более высокую и продолжительную стойкость вирусной нагрузки; следовательно, недостаточный клиренс вируса вместе с реактивным глиозом может продолжать нейровоспаление. Даже в легких случаях пневмония SARS-COV-2 вызывает гипоксию, которая сама по себе может спровоцировать или усилить воспалительную реакцию ЦНС. Церебральная гипоксия активирует ключевые факторы воспалительной транскрипции, включая NF-κB и индуцирующий фактор гипоксии, которые стимулируют перепроизводство провоспалительных мессенджеров, инициируют глиальную реактивность, индуцируют окислительное повреждение митохондрий и активируют промоторную область многочисленных микропрессов. воспаление. Чрезмерная глиальная реактивность в результате постоянного воздействия провоспалительных цитокинов также способствует потере синапса и гибели нейронов.
Влияние инфекции SARS-COV-2 на мозг связано с чрезмерным физическим и психологическим стрессом, который стимулирует ось гипоталамус-гипофиз-надпочечники, тем самым ухудшая нейровоспалительный статус. Продолжительность и частота воздействия стрессоров влияет на нейровоспаление. В этом смысле, хотя реакция на короткие и умеренные стрессоры может оказаться полезной, повторное или длительное воздействие сильных стрессоров усиливает воспаление. Воздействие на длительный стресс усиливает воспалительную реакцию благодаря высвобождению нескольких провоспалительных факторов, вызывающих дальнейшие сигнальные пути, включая транскрипцию NF-κB. Вклад глюкокортикоидов, ассоциированный с реакцией на стресс, в поддержании и стимулировании нейровоспаления является сложным, выходя за пределы эффектов, возникающих в результате активации сигналов по их рецепторам. Эксперименты с микроматрицами продемонстрировали, что глюкокортикоиды стимулируют экспрессию специфических генных профилей, тогда как одновременная коактивация глюкокортикоидных рецепторов и NF-κB-зависимая транскрипция индуцирует особую модель экспрессии генов, отличную от возникающей в результате отдельной активации каждого сигнала.
Нейровоспаление является важным этиологическим фактором для большого количества нервно-психических и нейрокогнитивных заболеваний, включая нейродегенеративные расстройства, депрессию, психозы, аутизм, злоупотребление наркотиками, нарушение сна и эпилепсию. В настоящее время нервно-психическое течение этой пандемии неизвестно, но, вероятно, будет значительным. На основании результатов исследований последних эпидемий корона-респираторных вирусов, SARS-COV-1 и MERS-COV, можно предположить, что значительный процент субъектов, выздоравливающих от пневмонии, не восстанавливают полностью свое прежнее эмоциональное состояние и когнитивные способности. Действительно, исследование нервно-психических последствий SARS-COV-1, проведенное через 30-50 месяцев после заражения, продемонстрировало возникновение 40% посттравматического стрессового расстройства (ПТСР), 36,4% депрессии, 15,6% обсессивного судорожного расстройства. . на тревожные расстройства. Кроме того, метаанализ среди пациентов с последствиями SARS-COV-1 со смешанными состояниями показал нейрокогнитивный дефицит к 18 месяцам после выписки, включая легкие когнитивные нарушения.
Учитывая эти доказательства, бремя длительного делирия и деменции после SARSCoV-2 может быть заметным, особенно для пожилых людей, которые более уязвимы к постинфекционным нейрокогнитивным последствиям. Средний возраст пациентов с тяжелым COVID-19 составляет около 63 лет, в то время как пациенты в возрасте до пятидесяти лет составляют всего 26% всех клинических случаев. Само старение является основным фактором риска когнитивных патологий и нейродегенерации; тяжелые системные заболевания, а также стресс провоцируют или ускоряют когнитивный спад у пожилых людей. В старческом мозге нейрогенез уменьшается, ухудшается синаптическая пластичность, уменьшается обмен веществ и повышается общая уязвимость мозга к экзогенным поражениям. Старение человеческого мозга также связано с дегенерацией и атрофией микроглии и астроцитов, что уменьшает гомеостатическую и нейропротекторную поддержку и снова повышает восприимчивость к патологии. Таким образом, заражение SARSCoV-2 (даже в умеренных клинических случаях) способствует когнитивным расстройствам с возникновением делирия, острым психозом, обострением легких когнитивных нарушений или ускорением деменции, связанной с различными нейродегенеративными состояниями, включая болезнь Альцгеймера. Нейрозожжение способствует патологическому развитию нейродегенерации и часто рассматривается как общая, даже объединяющая характеристика нейродегенерации, в то время как инфицирование мозга и ишемические поражения сами по себе могут спровоцировать нейродегенеративный процесс и спровоцировать деменцию.
Общепризнано, что системное воспалительное заболевание ускоряет когнитивные нарушения, что означает, что сама инфекция, как и нарушение врожденной иммунной системы, отвечает за когнитивные дефициты. Эпидемиологические наблюдения, а также невропатологический анализ подтверждают идею прямой корреляции между системными инфекциями, нейровоспалением и когнитивными расстройствами, такими как бреда и болезнь Альцгеймера. В этом контексте когортные исследования определили пневмонию как величайшую патологию, ответственную за ускорение и усиление когнитивного спада. В то же время прививки против бактерий или вирусов уменьшают риск постепенной эволюции деменции. Тесная корреляция между пневмонией и делирием у пожилых людей является давним наблюдением, а делирий, являющийся наиболее распространенным событием острой дисфункции мозга, является частым осложнением клинического прогрессирования COV-19, возможно из-за нейровирулентности, тяжелого периферического воспаления, глубокий стресс. Даже "социальное дистанцирование" и одиночество, которые переживают пожилые люди во время пандемии, способствуют возникновению психотических эпизодов.
COVID-19 и большое депрессивное расстройство
Системный и тканевый иммунный ответ способствуют патофизиологии многочисленных нервно-психических заболеваний путем модификации нейрохимической среды, синаптической передачи и пластичности, синтеза и секреции нейротрофических факторов, нейрогенеза и мозгового коннектома. В этом контексте большое депрессивное расстройство является одним из наиболее распространенных нервно-психических расстройств, связанных с воспалительным поражением головного мозга. Большое количество улик связывает симптомы депрессии с провоспалительными факторами и нейроглиальной недостаточностью. Эта ссылка касается конкретно подтипов депрессии, возникающих у пожилых людей. Старение оказывает существенное влияние на уровень и активность провоспалительных цитокинов в ЦНС. Системная инфекция сама по себе может вызвать серьезную депрессию у пациентов пожилого возраста из-за зависимого от возраста снижения иммунного гомеостаза. В частности, повышенный уровень интерлейкина-1β в сыворотке крови непосредственно коррелирует с появлением большого депрессивного расстройства позднего возраста. Подобным образом наблюдается корреляция между воспалительными факторами и некоторыми специфическими симптомами, например высокий уровень TNF-α и IL-2 ассоциируется с апатией и двигательным торможением, тогда как IL-6 ассоциируется с ангедонией и суицидальностью. Уровни цитокинов снижаются, когда пациенты восстанавливают нормальный уровень настроения и наоборот, цитокины остаются повышенными у пациентов, устойчивых к лечению.
Тяжелые случаи COVID-19 почти неизменно сопровождаются чрезмерным иммунным ответом хозяина, главным образом характеризуется значительным повышением уровня IL-6 в плазме крови, непосредственно коррелирует с неблагоприятным исходом заболевания. В то же время аномально высокие концентрации IL-6 были обнаружены в мозговой спинномозговой жидкости тех, кто пытался совершить самоубийство, у субъектов, страдающих либо депрессией, либо шизофренией, у пожилых пациентов с депрессией и у матерей с послеродовой депрессией. Большое количество доказательств показало, что изменения уровня IL-6 как в плазме, так и в головном мозге приводят к возникновению депрессии, хотя другие факторы, имеющие естественный или генетический характер, вносят важный вклад. В ЦНС ИЛ-6 действует как провоспалительный медиатор, способствующий синтезу и секреции дополнительных воспалительных факторов и белков острой фазы астроцитами и микроглией.
Таким образом, IL-6, вместе с TNF-α и IL-1β, можно рассматривать как один из основных регуляторов иммунного ответа мозга, тогда как астроциты и микроглия являются основными реагентами на IL-6, а также известными производителями IL-6, стимулированными повреждениями и патогенно-ассоциированными молекулярными структурами (включая вирусы и их компоненты), нейромедиаторами и провоспалительными мессенджерами. Физиологические уровни IL-6 в плазме крови у взрослых колеблются в пределах 1–10 пг/мл, тогда как при системном воспалении повышается до нескольких нг/мл; сообщалось о 114 и даже более высоких концентрациях для COVID 19.
Кстати, высокий уровень IL-6 был обнаружен в плазме крови, спинномозговой жидкости и предсмертной префронтальной коре субъектов с суицидальными намерениями, с нелетальными попытками самоубийства или самоубийствами. В то же время прямая корреляция не была найдена между концентрацией IL-6 в плазме и ликвором у лиц, пытавшихся осуществить суицид, а также такой корреляции не выявлено для баллов тяжести депрессии. Уровни IL-6 в циркуляции также коррелировали с суицидальным эндофенотипическим поведением, таким как расстройства свойств личности, агрессивность и импульсивность. Это согласуется с многочисленными выводами, доказывающими роль цитокинов в регуляции эмоций и поведения через взаимодействие с конкретными участками мозга и разными нейрональными путями. Пандемия COVID-19 привела к значительным изменениям в образе жизни и межличностных отношениях, осудив многих на длительное одиночество. Эти условия психосоциального стресса могут также губительно влиять на наиболее хрупких субъектов, влияя на их способность модулировать эмоции. Снижение контроля над импульсивностью и чувством страха в сочетании с воспалительными проблемами мозга может увеличить риск суицида.
COVID-19 и биполярное расстройство (БР)
Ненормальный баланс между провоспалительными (IL-6 и TNF-α) и противовоспалительными цитокинами в ЦНС и в плазме неоднократно наблюдался у пациентов с БР, что подтверждает мнение, что нейроиммунный ответ может быть важным фактором, способствующим этиопатогенезу этой болезни. В острых фазах БР или во время маниакального или депрессивного эпизода сообщалось об активации воспалительных каскадов, что многими, но не всеми, считалось характерным признаком острой болезни, а не устойчивым признаком заболевания. Установлено, что несколько цитокинов, таких как IL-1β, TNF-α, IL-6, интерферон-γ, увеличивают циркуляцию в острых фазах БР, параллельно снижая противовоспалительные факторы IL-10 и трансформируя фактор роста β-1, особенно в маниакальной фазе. .
Анализ присутствия провоспалительных молекул в ликворе у больных БР выявил противоречивые результаты. Несколько высокий уровень ликвора в IL-8, хемоаттрактантный белок 1 моноцитов (MCP-1/CCL-2) и легкая цепь нейрофиламентов были обнаружены у субъектов БР, хотя эти биомаркеры не коррелировали с результатом заболевания. Мета-анализ содержания цитокинов в ликворе у больных БР выявил повышенный уровень IL-1β, IL-8 продемонстрировал статистически незначительный подъем и изменений в отношении IL-6 не обнаружено.
Несоответствие между уровнями интерлейкинов и хемокинов в сыворотке крови и ликворе является другим спорным вопросом. Конечно, соблазнительно предположить, что это расхождение утрачено в COVID-19, поскольку перегрузка интерлейкинов и хемокинов, компрометация ГЭБ и активация резидентов ЦНС и вторжение в иммунные клетки усиливает нейровоспаление и способствует двунаправленному потоку воспалительных мессенджеров через проницаемый барьер. Однако такой сценарий остается крайне гипотетическим, и требуется гораздо больше исследований и анализов, чтобы выявить возможную связь вирусной инфекции в целом и COVID-19, в частности с БР.
COVID-19 и реактивный психоз
Широкий спектр нарушения регуляции иммунной системы, а также инфекций (вместе с обычно генетической уязвимостью, отклонениями в нейромедиаторах, стрессом и влиянием факторов окружающей среды, таких как жестокое обращение в детстве) признаются потенциальными патогенетическими факторами реактивного психоза. Усиленное воспаление при психозе подтверждено метаанализами, показывающими повышенную концентрацию цитокинов и их рецепторов при хронической шизофрении, а также у пациентов, не получавших лекарства в первом эпизоде психоза. Недавнее исследование, направленное на исследование провоспалительного профиля цитокинов у пациентов с эпизодами психоза, показало повышение регуляции IL-6, TNF-α и IL-1β, что не было обнаружено у здоровых братьев и сестер, предполагая, что знакомая уязвимость не участвует в генерации воспаление-ассоциированных психотических реакций. Пытаясь концептуализировать риск возникновения психоза у субъектов, инфицированных SARS-COV-2, следует подчеркнуть, что высокий уровень IL-6 коррелирует с уменьшением размера гиппокампа у шизофреников, по крайней мере, частично, ввиду их когнитивных дефицитов. Более того, повышенный уровень IL-6 был обнаружен в ликворе ликвора больных шизофренией. Еще более интригующим является наблюдение, что высокий уровень IL-6 у подростков положительно коррелирует с возникновением психоза в дальнейшей жизни.
COVID-19 и обсессивно-компульсивное расстройство
Растущее количество литературы сообщает о появлении навязчивых состояний у пациентов, недавно выздоровевших от вирусного энцефалита. Уже в 1930-х гг. Более трети случаев обсессивно-компульсивных расстройств (ОКР) были признаны органическими в патогенезе и связаны с энцефалитом фон Экономо.
Впоследствии в нейропсихиатрической литературе были раскинуты многочисленные сообщения о случаях заболевания: от обсессивных синдромов с постенцефалитическим паркинсонизмом до находящихся после энцефалита, у которых несахарный диабет сосуществовал с ОКР, до шести больных ОКР с вирусным анамнезом. Кроме этих ранних примеров, недавно были обнаружены высокие уровни иммунных комплексов вируса Борна и вирусных компонентов (белков, РНК) в крови и периферических одноядерных клетках больных ОКР, что усиливает представление о значительной связи между вирусной инфекцией и ОКР у предрасположенных субъектов . В этом сценарии, поскольку функциональная нейровизуализация, продемонстрированная ОКР, предполагает изменения в стриато-таламо-кортикальных цепях, было интересно, что активность этих цепей может влиять на вирусную инфекцию, возможно из-за препятствия передаче глутамата.
Вне всяких сомнений, иммунная дисфункция играет причинную роль в развитии ОКР в детстве, когда внезапный приступ навязчивых симптомов и тиков возникает после стрептококковой инфекции, с последующим продуцированием аутоантител против нейрональных антигенов базальных ганглиев, что придает представление о том, что изменения системы могут быть причастны к патологии этих расстройств. Многочисленные исследования показали корреляцию между уровнем провоспалительных цитокинов в циркуляции и ОКР. Увеличение концентрации IL-1β, IL-6 и TNF-α в крови у больных ОКР было выявлено по сравнению с нормальным контролем в паре по полу, возрасту и образованию. Эти выводы согласуются с результатами исследований, изучающих тех, кто не страдает сопутствующей патологией ОКР. Наблюдение об увеличении воспалительных цитокинов в исследовании, устранившем любые непонятные факторы, такие как тревожная или депрессивная сопутствующая патология или последствия психотропных препаратов, является более убедительной поддержкой идеи о том, что иммунологические отклонения способствуют происхождению ОКР. Таким образом, системное воспаление, являющееся отличительной особенностью COVID-19, может вызвать ОКР.
COVID-19 и эпилепсия
Литература сообщает об эпилепсии и нарушениях поведения как тесно связанные патологии. Действительно, психические заболевания чаще у пациентов с эпилепсией, чем в общей популяции, независимо от времени возникновения судорог, которые могли возникнуть до или после появления психических расстройств, что свидетельствует о взаимных отношениях и потенциально общей этиологии. Это интригующее сосуществование психических особенностей у больных эпилепсией не представляет собой случайности или обычной сопутствующей патологии, но, скорее всего, оно отражает взаимосвязанные патологические процессы. Нейрозожжение может намекать на основной механизм, разделяющий эпилепсия и психические расстройства, хотя и с четким участием нейрональных субстратов. Это делает любое жесткое разделение между эпилепсией и некоторыми психическими расстройствами менее жестким, поэтому мы включили эпилепсию в дискуссию относительно значительных поведенческих изменений и роли нейровоспаления в его патогенезе.
Связь между эпилепсией и нейровоспалением общепризнана. Устойчивый нейровоспалительный каскад, обусловленный нагрузкой цитокинов и повреждением ГЭБ, связан с глиальной реактивностью, синаптическими изменениями и образованием гипервозбудимых сетей с более низким порогом судорог, что способствует эпилептической активности. Эпидемиологические данные указывают на нейроинфекцию и системные инфекции как одну из основных причин приобретенной эпилепсии. Например, вирусный энцефалит увеличивает риск дальнейших судорог. Повышенные концентрации IL-1 были обнаружены в плазме крови и ликворе разного эпилептического фенотипа, что свидетельствует об этих свойствах, стимулирующих припадки цитокинов. Изменения в передаче ГАМК-ергической трансмиссии и уменьшение поглощения астроцитарного глутамата могут вызвать в зависимости от IL-1 увеличение восприимчивости к эпилепсии. Подобным образом, повышенный уровень IL-6 сообщался как в плазме, так и в ликворе у пациентов, страдающих широким спектром эпилептических проявлений, тогда как это увеличение концентраций коррелировало с тяжестью судорог. Возможность IL-6 способствовать эпилептогенезу еще больше подтверждается доказательствами того, что чрезмерная экспрессия IL-6 индуцирует аномальный иктогенез у мышей в гиппокампе. Пока не сообщается о связи между эпилепсией и COVID-19, однако, Американское общество эпилепсии уже предположило, что COVID-19 может увеличить риск внезапной неожиданной смерти при эпилепсии (SUDEP). Есть некоторые сообщения, указывающие на то, что инфекции, бактериальные или вирусные могут увеличить риск развития SUDEP. В настоящее время нет данных о связи между COVID-19 и SUDEP.
COVID-19 и посттравматическое стрессовое расстройство
Предполагается, что как только травма закончится и субъект больше не будет под давлением стресса, начинается путь устойчивого восстановления, поскольку время заживляет все раны. К сожалению, это не всегда так, поскольку у восприимчивых субъектов активный стресс стимулирует мозговые процессы, в результате которых травматические воспоминания внезапно снова возникают и нарушают психическое здоровье. Постоянство этих условий порождает посттравматическое стрессовое расстройство (ПТСР). ПТСР больше не классифицируется среди тревожных расстройств; это считается травмой или связанным со стрессовым расстройством. Патогенетическая связь между воспалением и ПТСР хорошо задокументирована. Из-за заметного влияния стрессовых факторов на иммунную систему неудивительно, что ПТСР связан с иммунным состоянием. Повышенная концентрация провоспалительных факторов наблюдалась как в системном кровообращении, так и в мозге в контексте ПТСР. Активация нейроглии, индуцированная тяжелыми или устойчивыми стрессорами, может стимулировать аберрантную секрецию провоспалительных сигналов, что может облегчить появление ПТСР. Данные метаанализов подтверждают значительное увеличение провоспалительных молекул у лиц с ПТСР, включая IL-6, TNF-α и IL-1β.
Уровни IL-10, противовоспалительного интерлейкина, также были повышены, вероятно, для попытки компенсировать воспалительные процессы, вызванные стрессом, дополнительно подчеркивая тесную связь между воспалением, стрессом и ПТСР. Возникновение ПТСР, как правило, было связано с возникновением слабой степени воспаления. Помимо изменений в цитокинах ПТСР также связан с усиленной экспрессией NF-κB, этот фактор транскрипции причастен к воспалительному процессу и его повышенная экспрессия коррелирует непосредственно с тяжестью ПТСР. Более того, ПТСР обычно сопровождается депрессией, а также тревогой, наркоманией и высокой частотой самоубийств, поскольку все эти состояния имеют общие воспалительные механизмы в своих патогенетических процессах. Однако остается выяснить, есть ли отношения во всех случаях взаимными и какие факторы, наряду с воспалительными, играют причинную роль в определении сопутствующих заболеваний. ПТСР может быть возможным результатом для больных COVID-19. Это вытекает не только из тяжести системного воспаления и вирусной инвазии в мозг, но также из тяжести стресса, вызванного неожиданной пандемией, для высокой смертности шокирующей.
Шизофрения и вирусная инфекция
Значительное количество психотических эпизодов после пандемии испанского гриппа подчеркнуло возможность увеличения частоты шизофренических расстройств у объектов, инфицированных SARS-COV-2. У пациентов с COVID-19 сообщалось о высоком уровне иммунореактивности коронавируса у пациентов с недавними наступлениями психотических эпизодов, а также серьезных нервно-психических осложнений, включая слуховые и зрительные галлюцинации, а также тяжелых бредов. Несмотря на то, что общепризнанное происхождение нейроразвития шизофрении, нельзя исключать других этиологических факторов, таких как прямое воздействие вирусной нейроинфекции или косвенный эффект иммунных аберраций, встречающихся у взрослых. Шизофрения также рассматривается как нейродегенеративная болезнь в зрелом возрасте, с усадкой и утратой нейронов, повреждением олигодендроцитов, изменениями синаптической связи, вероятно, связанными с когнитивными нарушениями. Хотя отсутствуют данные, непосредственно связывающие COVID-19 с риском шизофрении, частое возникновение психотических эпизодов подчеркивает необходимость дальнейших, более детальных исследований.
Выводы
Пандемия SARS-COV-2 создает длительный вызов, который не только поражает сердечно-дыхательную систему, но связывает системную инфекцию с нервно-психическими заболеваниями. Исследования предыдущих вирусных респираторных эпидемий показали начало широкого диапазона психических расстройств в течение и после инфекции. Пандемия испанского гриппа в 1918–1920 годах подтолкнула предположение о причинной роли вирусной инфекции в патогенетическом механизме поведенческих расстройств у биполярных и шизофренических субъектов. Карл Мэннингер одним из первых заявил, что его убедили, что деменция praecox (как в те времена называли шизофрению) является, в большинстве случаев, соматопсихозом, «психическими проявлениями энцефалита". В тот же период Якоб Касанин и Дж. В. Петерсен предположили, что «тщательный обзор некоторых ранних историй атипичных случаев шизофрении или аффективных расстройств может выявить предыдущий энцефалит».
В настоящее время существует мало предварительных исследований, рассматривающих нервно-психические осложнения COVID-19, однако, на основе результатов предыдущих эпидемий разных респираторных вирусов можно предположить повышенную частоту психических патологий как нежелательных последствий. Не только ОРВИ-COV-2 может проникнуть в мозг и вызвать прямое повреждение нейрональных сетей, опыт потенциально смертельного и неизлечимого COVID-19 является причиной сильного дистресса, который может вызвать долгосрочные изменения поведения или усугубить уже существующие психические заболевания. Здесь мы обозначили возможные нервно-психические осложнения, которые могут возникнуть у лиц, инфицированных SARS-COV-2. Пациенты с COVID-19 могут иметь широкий спектр нервно-психических симптомов, возникающих вследствие системного воспаления, воздействия на ЦНС цитокинов, заражения нервных клеток SARS-COV-2, нейровоспаления, глиальной дисфункции или аберрантных эпигенетических модификаций генов, связанных со стрессом. Этот обзор имел целью привлечь особое внимание к психиатрическим аспектам COVID-19, поскольку сведение к минимуму их актуальности, утверждая, что иногда "ненормальная реакция на ненормальную ситуацию - это нормальное поведение" может быть непростительной ошибкой.
Notes
- Holland, H., 1839, Medical Notes and Reflections, Haswell, Barrington, and Haswell, Philadelphia, p. 136.
- Ravenholt, R. T., and Foege, W. H., 1982, 1918 influenza, encephalitis lethargica, parkinsonism, Lancet, v. 2, p. 863.
References
Со ссылками на источники информации можно ознакомиться в оригинале статьи: https://www.nature.com/articles/s41398-020-00949-5.pdf
Программы Universum.Clinic :
Программа сопровождения и лечения Клиентов с коронавирусной инфекцией